
| Российский химико-аналитический портал | ::: портал химиков-аналитиков ::: химический анализ и аналитическая химия в фокусе внимания ::: |
 |
|
| ANCHEM.RU » Литература » Справочные, учебные материалы / книги » ... |
Методы жидкостной хроматографии и твердофазной экстракции
»
... 5. Хиральная высокоэффективная
|
|
Источник |
Тип селектора |
Хиральный селектор |
|
Натуральные |
Протеины |
Альбумины |
|
Гликопротеины |
||
|
Энзимы |
||
|
Олигосахариды |
α-Циклодекстрин |
|
|
β-Циклодекстрин |
||
|
γ-Циклодекстрин |
||
|
Антибиотики |
Ванкомицин |
|
|
Тейкопланин |
||
|
Ристоцетин |
||
|
Алкалоиды |
Хинин |
|
|
Хинидин |
||
|
Полусинтетические |
Модифицированные олигосахариды |
Дериватизированные циклодекстрины |
|
Модифицированные полисахариды |
Карбаматы полисахаридов |
|
|
Сложные эфиры полисахаридов |
||
|
Модифицированные низкомолекулярные природные соединения |
Ионообменные селекторы |
|
|
Производные пролина и других аминокислот (лигандообменные селекторы) |
||
|
Синтетические |
Низкомолекулярные синтетические соединения |
Пиркловские фазы (фазы браш-типа) |
|
Синтетические полимеры |
Сшитые тартрамиды |
|
|
Полиакрилаты и полиакриламиды |
||
|
Импринтные материалы |
С практической же точки зрения наиболее удобно рассмативать их с позиции частоты применения.
Безусловно, наиболее универсальными и широко применяющимися являются фазы с хиральными селекторами на основе модифицированных полисахаридов (карбаматов и эфиров). Считается, что, имея линейку трех или четырех фаз этого типа (Chiralcel OD, AD, OJ, AS), можно разделить до восьмидесяти процентов всех хиральных соединений (рис. 5.1.1).
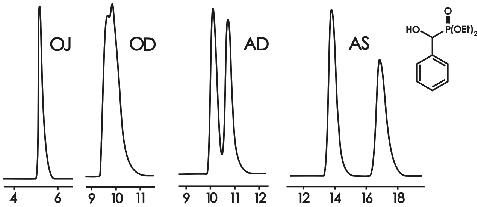
Рисунок 5.1.1. Разделение рацемата (структурная формула приведена на рисунке) на четырех различных фазах Chiralcel. Элюент гексан-изопропанол 100:10. Хроматограмма получена Ильиным М.М. (лаборатория ССП ИНЭОС РАН).
Эти неподвижные фазы получают прививкой модифицированных полисахаридов на силикагельную основу. Производство налажено фирмой Diacel Chemical Industies, которая выпускает их под общим названием Chiralcel. Основными фазами серии являются Chiralcel OD (OD-H, OD-R, OD-RH), Chiralcel AD (AD-H, AD-RH), Chiralcel OJ (OJ-H) и Chiralcel AS-H (AS-RH) (рис. 5.1.2.). Большинство разделений проводятся в нормально-фазовом режиме, однако в последнее время широко начал применяться и обращенно-фазовый вариант, для которого были разработаны специальные модификации фаз (их названия включают аббревиатуру R, reversed, например, Chiralcel OD-RH).
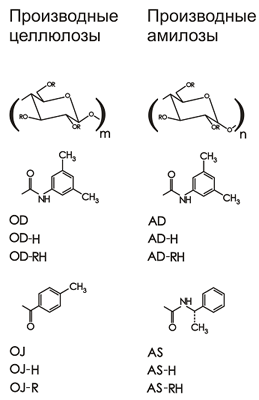
Рисунок. 5.1.2. Модификации фаз Chiralcel. Префикс «O» - производное целлюлозы, префикс «А» - производное амилозы.
Для разделения энантиомеров водорастворимых соединений широко применяются фазы с привитыми антибиотиками. Производство налажено фирмой Astec, которая выпускает их под общим названием Chirobiotic: Chirobiotic V с привитым антибиотиком ванкомицином, Chirobiotic R с ристоцетином, Chirobiotic T с привитым тейкопланином и Chirobiotic TAg – его производным. Эти фазы, первоначально разработанные для разделения аминокислот, прекрасно справляются с разделением многих гидрофильных хиральных соединений (рис. 5.1.3).
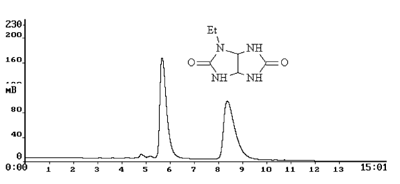
Рисунок 5.1.3. Разделение гидрофильного рацемата на фазе Chirobiotic TAg. Элюент метанол-вода 1:1. Хроматограмма получена Ильиным М.М. (лаборатория ССП ИНЭОС РАН)
Гораздо реже для разделения водорастворимых соединений применяются фазы с привитыми протеинами (табл. 5.1.2). Недостатками таких фаз является невысокая универсальность, эффективность и стабильность. В то же время, для некоторых соединений, структура которых сходна со структурой антигенов, фазы с привитыми протеинами способны проявлять непревзойденную селективость вплоть до α = 10-30 и выше.
Таблица 5.1.2. Неподвижные хиральные фазы с привитыми протеинами.
|
Протеин |
Коммерческое название |
Производитель |
|
BSA (бычий альбумин) |
Resolvosil BSA-7, BSA-7PX |
Nagel |
|
Ultron ES-BSA |
Shinwa Chemical Industries |
|
|
Chiral BSA |
Shandon |
|
|
HAS (человеческий альбумин) |
Chiral HAS |
Shandon |
|
Chiral-HSA |
ChromTech AB |
|
|
AGP (α1-гликопротеин) |
Chiral-AGP |
ChromTech AB |
|
OMCHI (овомукоид яичного белка) |
Ultron ES-OVM |
Shinwa Chemical Industries |
|
AVI (авидин) |
Biotic AV-1 |
GL Sciences |
|
CBH I (целлобиогидролаза I) |
Chiral-CBH |
ChromTech AB |
|
Пепсин |
Ultron ES-PEPSIN |
Shinwa Chemical Industries |
Значительная часть хиральных разделений проводится на фазах браш-типа (Пиркловского типа). Хиральными селекторами служат низкомолекулярные энантиомеры, привитые на силикагельную основу. Фазы браш-типа, как правило, применяются для нормально-фазовых разделений. Исключение составляют фазы с привитыми алкалоидами, которые применяются для ионообменных хиральных разделений.
Одной из достаточно популярных фаз Пиркловского типа для нормально-фазовых определений является Whelk-O,1 фирмы Regis; структурная формула хирального селектора приведена на рисунке 5.1.4.
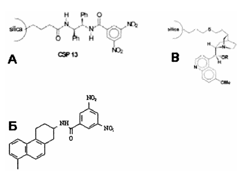
Рисунок 5.1.4. Хиральные селекторы наиболее широко применяемых фаз Пиркловского типа. (а) Pirkle ULMO, (б) Whelk-O,1, (в) фаз с привитым хинином.
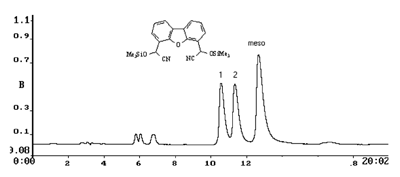
Рисунок 5.1.5. Разделение пары энантиомеров и мезо-формы соединения (структура приведена на рисунке) на фазе 250х4.6 Whelk-O,1. Элюент гексан-изопропанол 100:4. Хроматограмма получена Ильиным М.М. (лаборатория ССП ИНЭОС РАН).
К хиральным фазам на основе синтетических полимеров можно причислить Kromasil Chiral DMB и Kromasil Chiral TBB производства EKA Chemicals, полученные закреплением диметилбензоил- и третбутилбензоил- модифицированных тартрамидных полимеров на силикагельную основу. Эти фазы применяются для нормально-фазовых разделений (рис. 5.1.6).
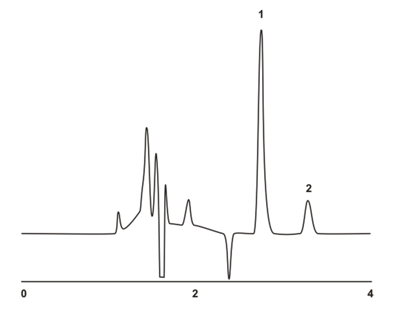
Рисунок 5.1.6. Разделение N,N’-ди(2,4-динитробензил)-транс-1,2-диаминоциклогексана на фазе Kromasil Chiral DMB. Элюент гексан-этилацетат 85:15.
Для разделения широкого спектра хиральных веществ до недавнего времени широко применялись фазы на основе циклодекстринов, привитых на силикагельную основу. В настоящее время применение этих фаз в значительной мере сократилось.
Циклодекстриновые фазы выпускаются фирмой Astec и носят общее название Cyclobond. Применяемые для прививки циклодекстрины отличаются прежде всего размером олигосахаридного цикла: наименьшим является α- и наибольшим – γ-циклодекстрин; наиболее универсальными являются фазы на основе среднего по размеру β-циклодекстрина. Фазы на основе α-, β- и γ-циклодекстринов обозначаются как Cyclobond I, Cyclobond II и Cyclobond III соответственно. Применяются также модификации этих фаз с дериватизированными циклодекстринами.
Примечательно, что в оригинальных источниках циклодекстриновые фазы предлагалось назвать, по аналогии с Пиркловскими фазами, Армстронговскими по фамилии их изобретателя.
Динамическим модифицированием обращенных фаз N-гексадецил-L-гидроксипролином с последующей пропиткой солью меди (II) получают фазы для лигандообменной хиральной хроматографии. Именного названия этот метод не имеет, однако сам модификатор, N-гексадецил-L-гидроксипролин, называется модификатором Даванкова. Лигандный обмен применяется для хирального разделения α-аминокислот, α-гидроксикислот и их производных.
Первое полное разделение энантиомеров методом жидкостной хроматографии (этим соединением был пролин) было осуществлено именно методом лигандообменной хроматографии на полистирольной смоле со включенным L-пролином (В.А. Даванков в соавторстве с С.В. Рогожиным, патент 1968 г.).
Одна из особенностей хиральной хроматографии состоит в том, что для успешного разделения адсорбат должен взаимодействовать с адсорбентом по крайней мере в трех точках. Иначе говоря, в оптимальном варианте должно достигаться множественное взаимодействие наиболее удерживаемого энантиомера с хиральной полостью. Только в этом случае разница в энергии адсорбции энантиомеров будет значительной, достаточной для их хроматографического разделения (разница в энергии адсорбции пропорциональна логарифму селективности).
Таким образом, для повышения универсальности хиральных фаз разработчиками проводится поиск таких селекторов, которые обеспечивали бы по возможности максимально возможное количество взаимодействий с адсорбатами различных классов. Для тестирования селективности хиральных фаз существуют даже специальные наборы модельных веществ.
Селекторы современных хиральных фаз способны к различным типам взаимодействий. В результате, удерживание на хиральных фазах, как правило, определяется суммой различных типов. Вклады различных типов могут быть сопоставимы по величине, при этом их величина может существенно различаться для адсорбатов даже сходной структуры.
Так, в нормально-фазовых условиях большинство типов хиральных фаз могут удерживать соединения по нормально-фазовому и квази-нормально-фазовому типам одновременно. В этом случае для полярных адсорбатов без мощных ароматических систем в большей мере применимы закономерности нормально-фазовой хроматографии, а для неполярных ароматических адсорбатов – закономерности квази-нормально-фазовой хроматографии. Наиболее ярко эти закономерности отслеживаются на полисахаридных фазах типа Chiracel OD и Пиркловских фазах типа Whelk-O,1, поскольку такие фазы содержат в своей структуре как полярные функциональные группы, так и мощные ароматические системы.
Тейкоплаиновые и ванкомициновые фазы в гидрофильном режиме способны удерживать адсорбаты по нормально-фазовому, обращенно-фазовому и ионообменному типам. Выявить закономерности изменения удерживания и селективности разделения в зависимости от состава элюента на этих фазах чрезвычайно сложно.
Успешность разделения пары энантиомеров на определенной хиральной фазе зависит от нескольких факторов. Прежде чем начать их рассматривать, обратимся к понятию хиральной полости, которым оперируют при построении моделей хирального распознавания.
Дискриминация (распознавание) энантиомеров на хиральных неподвижных фазах становится возможной по причине хиральности центров адсорбции энантиомеров. Величины энергий взаимодействия адсорбционного центра с каждым из энантиомеров различаются – соответственно, различаются и времена удерживания энантиомеров.
Адсорбционный центр хирального селектора, включая его микроокружение (которое также участвует в связывании молекулы энантиомера), называется хиральной полостью. Согласно теории, для распознавания энантиомера адсорбционным материалом необходимо, по крайней мере, его трехточечное взаимодействие с хиральной полостью.
Каждый из типов хиральных фаз характеризуется индивидуальной структурой хиральных полостей. Как было установлено в специальных исследованиях, для полисахаридных фаз хиральной полостью может являться каждая структурная единица спирали, то есть каждый модифицированный остаток глюкозы. Для фаз браш-типа хиральной полостью является молекула селектора и ее окружение (включая спейсер). Для циклодекстриновых фаз хиральной полостью является молекула циклодекстрина, образующая с адсорбатами комплексы включения.
Достаточно крупная молекула селектора может иметь несколько хиральных полостей, даже для одного энантиомера. Так, молекула альбумина HAS содержит один сайт связывания с R-ибупрофеном, и по крайней мере два – с S-ибупрофеном.
Отсутствие разделения энантиомеров при любой эффективности, то есть α = 1, может объясняться несколькими причинами.
Очевидно, что разделения энантиомеров не происходит, если адсорбаты не проникают в хиральную полость. В свою очередь, это может быть вызвано тем, что:
размер молекулы адсорбата, или размер хиральной части его структуры, больше размера хиральной полости (рис. 5.2.1);
адсорбат не может проникнуть сквозь адсорбционный слой полярного модификатора, блокирующий хиральную полость (в нормально-фазовом режиме).
Даже если адсорбат проникает в хиральное окружение, дискриминация энантиомеров может не происходить, так как:
при связывании не достигается «трехточечная» фиксация адсорбата;
адсорбат связывается с хиральной полостью преимущественно нехиральным участком.
В случаях 1 и 3 разделение принципиально невозможно осуществить на выбранной неподвижной фазе. В случае 4 разделение можно провести, если значительно изменить хроматографическую систему. К примеру, можно перейти от нормально-фазовой системы к обращенно-фазовой или наоборот, если выбранный тип фазы это позволяет. Добиться разделения путем коррекции состава подвижной фазы и/или температуры можно только во втором случае.
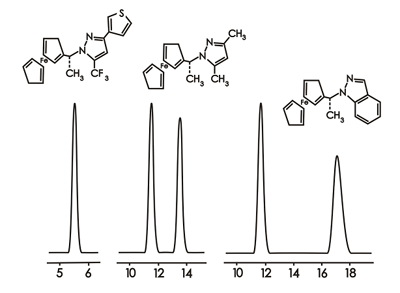
Рисунок 5.2.1. Разделение ряда производных ферроцена на фазе 250x4.6 Chiralcel OD-H. Элюент гексан-изопропанол 100:4. Хроматограмма получена Ильиным М.М. (лаборатория ССП ИНЭОС РАН).
Разделение уменьшается справа налево, при замене достаточно компактного и способствующего удерживанию ароматического кольца на две метильные группы, а затем исчезает при замене одной метильной группы на более объемную трифторметильную, а другой – на более объемную тиофенильную.
Некоторые структуры могут быть достаточно «трудными» для хирального разделения методом жидкостной хроматографии (рис. 5.2.2). Можно выделить несколько признаков, по которым «трудные» рацематы быстро распознаются:
Заместители при хиральном центре – небольшие и неполярные, примерно одинакового объема. Пример: хлор и метил.
Заместители при хиральном центре очень похожи, особенно вблизи хирального центра.
Молекула адсорбата достаточно крупная, с разветвленными алифатическими заместителями. В случае неудачного разделения в нормально-фазовом режиме можно попробовать разделить такую структуру в обращенно-фазовой системе.
Хиральный центр в составе крупной молекулы удален от ее наиболее полярного фрагмента или фрагмента с наиболее мощной ароматической системой.
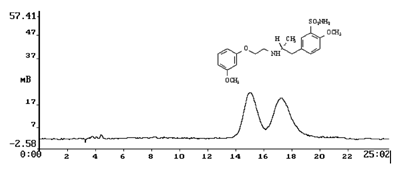
Рисунок 5.2.2. Пример разделения «трудного» рацемата на фазе 250x4.6 Chiralcel
AS-H.
Элюент гексан-этанол-триэтиламин 50:50:0.1.
Хроматограмма получена Ильиным М.М. (лаборатория ССП ИНЭОС РАН).
Хиральный центр одинаково удален от наиболее полярной части молекулы (вблизи сульфамидной группы) и от ароматических фрагментов (одно и другое ароматические кольца с заместителями). Только один заместитель при хиральном центре способен взаимодействовать с адсорбентом (аминогруппа).
Разделение было достигнуто только на одной фазе, Chiralcel AS-H, причем оно не было стабильным – селективность зависела от трудно контролируемых параметров.
В том случае, когда недостаточная селективность разделения энантиомеров обусловлена образованием адсорбционного слоя полярного модификатора, блокирующего хиральную полость, разделение может быть, в принципе, улучшено путем изменения состава подвижной фазы и/или температуры. Такие случаи характерны, в большей или меньшей степени, для всех хиральных фаз в нормально-фазовом режиме хроматографирования. Общий принцип улучшения разделения здесь можно сформулировать следующим образом: следует создать такие условия, в которых адсорбционный слой не образуется, или происходит его замена на адсорбционный слой другого модификатора, не препятствующего разделению.
Примером хиральной фазы, к которой этот принцип применим в полной мере, является Kromasil Chiral DMB. Фаза, как было упомянуто, получена закреплением диметилбензоил-модифицированного тартрамидного полимера на силикагельную основу. Для этой фазы вклад квази-нормально-фазового типа удерживания невелик, значительно меньше, чем для типичных Пиркловских фаз. В результате, хиральное распознавание происходит по большей части за счет водородных связей амидных групп и влияния стерического фактора. Стоит также отметить, что и полярность этой фазы невысока – меньше, чем у нитрильной фазы, и значительно меньше, чем у силикагеля.
Применение спиртов (особенно с разветвленными заместителями) как полярных добавок приводит в этом случае к резкому уменьшению селективности разделения. По этой причине, в качестве полярных добавок при применении Kromasil Chiral DMB применяют эфиры. Спирты, по-видимому, блокируют амидные функциональные группы – при этом блокируются и хиральные полости. Этот эффект большей частью связан именно с поверхностью, поскольку для его проявления достаточно совсем небольшой концентрации спиртов в элюенте. Оптимальной полярной добавкой для Kromasil Chiral DMB является метил-третбутиловый эфир, который из-за трет-бутильного заместителя обладает наименьшей модифицирующей способностью даже среди эфиров.
Подобные закономерности характерны также и для Пиркловских, и для полисахаридных фаз (рис. 5.2.3). Многие исследователи отмечали, что селективность разделения на них увеличивается при переходе от протонных полярных добавок к апротонными.
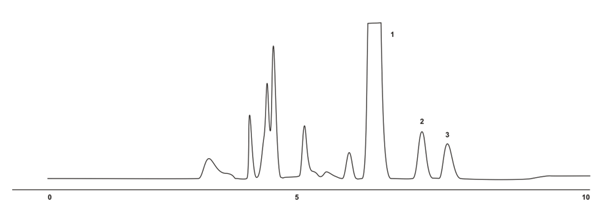
Рисунок 5.2.3. Разделение рацемата аллилметилфенилкарбинола (2,3) на фазе 250x4.6 Chiralcel OD-H. Элюент гексан-хлороформ-уксусная к-та 95:3:2.
При применении в качестве элюента системы гексан-изопропанол разделения не наблюдалось. Разделение было достигнуто при замене изопропанола на уксусную кислоту. Добавление в элюент хлороформа было вызвано необходимостью разделения рацемата (2, 3) от пика ацетофенона (1).
Большое число случаев влияния адсорбционного модифицирования и перемодифицирования на селективность разделения энантиомеров выявлено для полисахаридных фаз серии Chiralcel. Эти фазы характеризуются как наиболее высоким среди хиральных фаз вкладом квази-нормально-фазового типа удерживания (поскольку содержат замещенные ароматические фрагменты), так и чрезвычайно высокой полярностью, сравнимой или даже большей, чем у силикагеля. Еще одна их особенность связана с тем, что производителем не рекомендуется применять элюенты на основе иных растворителей, кроме гексана, спиртов и воды (возможны небольшие добавки кислот и аминов). Соответственно, при разделении полярных соединений без спиртов не обойтись. Селективность разделения можно увеличить, применяя спирты с меньшим заместителем, или добавляя в элюент гексан-спирт небольшие количества воды. В последнем случае происходит перемодификация поверхности адсорбента, то есть молекулы спирта, блокирующие хиральные полости, заменяются на молекулы воды. Следует также заметить, что подобный процесс происходит и при замене одного спирта на другой, поскольку при этом нередко наблюдается значительное изменение селективности вплоть до инверсии порядка элюирования энантиомеров.
Один из наиболее ярких примеров увеличения разделения энантиомеров вследствие перемодификации поверхности наблюдался при анализе бензимидазола тимопразола, проведенного на фазе Chiralpak AD при варьировании доли метанола в подвижной фазе гексан-изопропанол 80:20. При составах элюента гексан-изопропанол-метанол от 80:20:0 до 80:15:5 разделение едва намечается. При достижении концентрации метанола в элюенте 5% наблюдается резкий скачок времени удерживания второго энантиомера (более удерживаемого) при неизменном времени удерживания первого энантиомера. В результате, происходит резкое увеличение селективности разделения, которое не изменяется при дальнейшем увеличении концентрации метанола в элюенте.
Такие же случаи наблюдались и с применением воды в качестве перемодификатора. Иногда эти случаи бывали курьезными, как, к примеру, при разработке методики разделения полярных амидов 2-оксо-3-пиперидин-ацетамидов на фазе Chiralcel OD. Разделение, полученное в одной лаборатории на элюенте гексан-этанол 90:10 с 0.1% ТФУ не воспроизвелось в другой лаборатории – разделения не наблюдалось. Оказалось, что во второй лаборатории этанол был абсолютированный, тогда как в первой – обычный азеотроп с водой. Таким образом, в первом элюенте содержалось еще порядка 0.38% воды, за счет которой и достигалось полное разделение.
Добавление воды не всегда приводит к увеличению селективности. Отмечены случаи, когда удерживание и селективность очень слабо зависят от концентрации воды в диапазоне 1-2 г/л; такая зависимость наблюдалась для α-гидроксиметопролола на фазе Chiralcel OD. По всей видимости, такой полярный адсорбат способен «пробить» любой адсорбционный слой.
При увеличении концентрации воды удерживание второго энантиомера может уменьшаться при неизменном времени удерживания первого, что приводит к уменьшению селективности. Такая ситуация наблюдалась при хроматографировании метопролола на фазе Chiralcel OD. Метопролол менее полярен, чем α-гидроксиметопролол, и именно этим можно объяснить то, что вода в данном случае уже выступает как модификатор, блокирующий хиральные полости.
Важным параметром, который необходимо по возможности контролировать при проведении разделений на полисахаридных фазах, является температура. Нередки случаи, когда при изменении температуры происходило изменение селективности вплоть до инверсии порядка элюирования энантиомеров. В целом же, несмотря на такие «тонкости», полисахаридные фазы остаются на сегодняшний день наиболее универсальными и эффективными хиральными неподвижными фазами.
| ЖУРНАЛ | ЛАБОРАТОРИИ | ЛИТЕРАТУРА | ОБОРУДОВАНИЕ | РАБОТА | КАЛЕНДАРЬ | ФОРУМ |
| Copyright © 2002-2022 «Аналитика-Мир профессионалов» |
Размещение рекламы / Контакты |